Amikor meglátja a cukorbetegség visszahívásáról szóló fejléceket, és rájön, hogy az orvostechnikai eszközére hatással lehet, pánik támadhat.
A Medtronic inzulinpumpákkal és az Insulet Omnipod DASH rendszerével kapcsolatos legújabb termékbiztonsági hírek fényében (lásd a részleteket alább) elkezdtünk gondolkodni az események láncolatán, amely a címsorokat követi:
- Mi van, ha az ügyfelek aggódnak a termék további használata miatt?
- A vállalat világosan kommunikál és megfelelő ügyfélszolgálatot nyújt?
- Az egészségbiztosító társaságok törődnek-e azzal, ha az általuk lefedett vagy ajánlott termék lehetséges veszélyeket jelent?
- Hogyan reagálnak az orvosok és a cukorbetegséggel foglalkozó szakemberek aggodalommal a betegekre?
Mindez nemrégiben érkezett haza Paul Dobbertin, egy régóta chicagói külvárosban élő 1-es típusú ember számára, aki aggódni kezdett a Medtronic inzulinpumpa miatt, miután a média sokaságát látta, miután a közelmúltban az FDA figyelmeztetett egy termék visszahívására. Telefonált a cégnek, és harcolt egy csereeszköz megszerzéséért, annak ellenére, hogy az ügyfélszolgálat kicsinyítette a helyzetet, és ragaszkodott ahhoz, hogy egységét nem kell cserélni.
"Igazunk van, ha aggódunk" - mondja. "A rendszer minden részletének kezelése az 1-es típusú cukorbetegséggel együtt sok munka és költséges, anélkül, hogy további gondot okozna a hibás felszerelés és az ismert probléma."
Az eszköz felidézi: Amit tudnia kell
Először is ne keverje össze magát az ezekben a helyzetekben használt eltérő nyelvvel. A „visszahívás” szó nem mindig azt jelenti, hogy vissza kell küldenie egy terméket. Vannak „korrekciós” értesítések, „piaceltávolítások” és egyéb kapcsolódó címkék is. Lásd ezt az útmutatót az FDA definícióinak a különböző esetekről.
Az FDA elmagyarázza, hogy a legtöbb visszahívás „önkéntes cselekvés”, amelyet a gyártók és a forgalmazók hajtanak végre a közegészség védelmének felelősségének részeként, amikor bizonyos termékek sérülésveszélyt jelenthetnek vagy egyéb módon hibásak.
A legtöbb esetben csak bizonyos termékcsomagokat (meghatározott modelleket vagy cikkszámokat) érintenek. Tehát leggyakrabban eseti értékelés, hogy indokolt-e visszatérés egy adott egységre, ha a kérdéses probléma fennáll.
Itt találhatók a legutóbbi, 2020 elején bejelentett cukorbetegség-visszahívások részletei:
Medtronic Minimed 600 sorozatú inzulinpumpák: Rögzítőgyűrű visszahívása
A Minimed 600 sorozatú készülékeket a szivattyú tetején lévő apró rész érinti, amelyet rögzítőgyűrűnek neveznek, és amelynek állítólag biztonságban kell tartania az inzulintartályt a szivattyú belsejében. A meghibásodás megrepedhet vagy meglazulhat, megzavarhatja az inzulinadagolást, és esetleg oda vezethet, hogy a felhasználó több vagy kevesebb inzulint kap, mint kellene. Ez nem vezetne a tartály kiürüléséhez, mondja a Medtronic, de az inzulin beadásának késedelmét vagy gyorsabb, ütemezett bolust okozhat, amely eltér a vártól.

A Medtronic eredetileg 2019. november 21-én sürgősségi biztonsági értesítést adott ki erről a kérdésről, és erről értesítette az FDA-t. Abban az időben a vállalat a szabályozókkal már kidolgozta az eszköz potenciálisan hibás részeinek kezelésére vonatkozó cselekvési tervet.
Fontos, hogy nem ritka, hogy a gyártó biztonsági riasztást vagy értesítést ad ki, majd az FDA néhány hónappal később visszahívási besorolást ad ki. Ez történt itt, amikor az FDA 2020. február 12-én kiadta az 1. osztályú visszahívást, és ezt jelölte ki az általuk kiadott legkomolyabb típusú eszköz-visszahívásnak.
Hány eszközt érint?
Összesen 322 005 eszköz érintett, beleértve:
- a Minimed 630G szivattyúk összes része 2016 szeptembere és 2019 októbere között került forgalomba
- A 670G hibrid zárt hurok rendszer minden része 2017 júniusa és 2019 augusztusa között került forgalomba
Sérülés vagy haláleset?
Az FDA cégadatokon alapuló jelentése szerint a Medtronic 26 421 panaszt kapott a rögzítőgyűrű meghibásodásával kapcsolatban, mivel ezeket az inzulinpumpa-tételeket elosztották. Ezen adatok között 2175 „sérülés” és egy lehetséges haláleset szerepel.
Yikes! az első válasz, amikor meglátjuk ezeket a számokat. De aggodalomra ad okot, a Medtronic hangsúlyozza, hogy az adatok félrevezetőek lehetnek, ha azokat a kontextusból kivesszük. A „sérülések” címkével ellátott, összesen 2175 incidensből, amely magas vagy alacsony glükózszintet tartalmaz, 94 százalékot (összesen 2 045) „a beteg saját maga orvosolt, és nem igényelt orvosi beavatkozást”. A bejelentett egy halálesetet illetően nincs meggyőző bizonyíték arra, hogy laza, sérült vagy hiányzó rögzítőgyűrűvel lenne összefüggésben. De az sem zárható ki.
Korábbi, a termék-visszahívásokról szóló részletes tudósításunk során a DiabetesMine beszélgetett az FDA bennfenteseivel és a cég tisztviselőivel, akik óvatosságra intettek a visszahívási számok megfelelő kontextusban történő vizsgálata kapcsán - főleg, hogy az FDA „nemkívánatos események” adatbázisa korántsem tökéletes.
„Nem csak a visszahívások számát nézheti meg, és csak ezek alapján tehet következtetéseket. Kontextusba kell venned, mi volt a visszahívás, hogyan találták meg, és mi zajlott még akkoriban a céggel. Kívülről ezt nehéz megtenni, mert nem folytatják ezeket a beszélgetéseket és összefüggéseket. ”- figyelmeztet Dr. Courtney Lias, az FDA kémiai és toxikológiai eszközökkel foglalkozó részlegének igazgatója.
Eközben D-közösségünk az elmúlt hónapokban tele volt Medtronic biztonsági figyelmeztetésekkel: az FDA november közepi riasztásáról az idősebb inzulinpumpákról és a kiberbiztonságról, a szövetségi perről szóló híradásokig egy floridai nő miatt, aki meghalt 2 évekkel korábban, mint lehetséges melléktermék egy Minimed 530G rendszer használatával, amelynek visszahívását egy esetleg hibás infúziós helyhez kötötték.
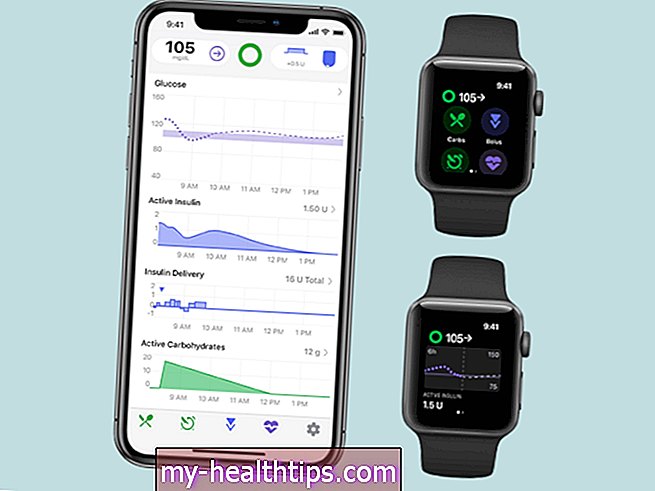
Omnipod DASH vezérlő egység: Szoftverhiba
A Medtronic 600 sorozat visszahívási bejelentésétől számított egy napon belül az Insulet orvostechnikai eszközökkel kapcsolatos korrekciós figyelmeztetést adott ki a tubularis Omnipod DASH tapaszpumpáról és a rendszer vezérléséhez használt személyes diabéteszkezelőjéről (PDM). Az elővigyázatossági intézkedésként leírt értesítés szerint távoli lehetőség van arra, hogy a PDM „helytelen információk alapján javasolhat inzulin bolusmennyiséget”, és ez túl sok vagy túl kevés inzulin beadását eredményezheti.
A kérdés konkrétan a bolus kalkulátor funkcióval foglalkozik, amelyet az élelmiszer- és korrekciós dózisok kiszámításához használnak az aktuális vércukorszint (BG) értéke és a felhasználó fedélzetén lévő inzulin (IOB) alapján. Normális esetben a PDM megakadályozza, hogy a 10 percnél régebbi leolvasást alkalmazzanak a számításokban. De ezzel a hibával régebbi adatokat gyűjtenek.
A probléma az 1.0.50-es és korábbi verziójú szoftverekre vonatkozik (a PDM Névjegy menüjéből kiderül, melyik verzióval rendelkezik).
A riasztás idején 11 panasz érkezett erről a kérdésről, és Insulet szerint nem történt személyi sérülés. És ez nem azt jelenti, hogy nem használhatja a DASH PDM-et - csak arra kell vigyáznia, hogy a bolus számológép használata során aktuális BG értéket adjon meg.
A riasztás szerint szoftverfrissítést fejlesztenek a probléma megoldására, amely várhatóan 2020 márciusában válik elérhetővé. A javítással ellátott új PDM-eket az érintett ügyfeleknek szállítják, és a vállalat azt mondja, hogy kapcsolatba lép azokkal az ügyfelekkel, amikor itt az ideje hajó.
Természetesen e megnyugtatások ellenére a cukorbetegek (PWD) elhúzódó kérdések és aggodalmak lehetnek.
Illinois inzulinpumper "nem élne a félelemmel"

Az egyik az illinoisi Dobbertin az 1990-es évek közepe óta használta a Minimed inzulinpumpát, és pár éve a 670G-n volt. Bár összességében nem volt teljesen elégedett annak egyszerű használatával, a minőségbiztosítás csak 2019 novemberében vált számára sürgetővé.
Annak ellenére, hogy Medtronic biztonsági riasztást kapott, és a cég megnyugtatta, hogy minden rendben van, Dobbertin aggódni kezdett, hogy az FDA visszahívási értesítésében a legfrissebb híreket látva hatást gyakorolhat a 670G készülékére.
További információkért felhívta a Medtronic ügyfélszolgálatát. Egy előre rögzített üzenet részletezte a visszahívást, és online kitöltötte az űrlapot. Levette a szivattyút, és egy fiókba tette, és szükség szerint több napi injekciót (MDI) váltott ki. Az egész napos válasz nélküli válaszadás után visszahívta az ügyfélszolgálatot, hogy értesüljön a látottakról.
"(A képviselő) a jelentett hírek nagy részét hibásnak minősítette, és azt mondta, hogy a szivattyút valójában nem hívták vissza" - mondta Dobbertin a DiabetesMine-nek. - Ez csak jobban összezavart. Úgy tűnt, hogy az online hírek - a CNN, az NBC, a BBC és még az FDA is - mást állítanak. Tudom, hogy a hírek elcsavarodnak, de az a tény, hogy ennyi sérülést jelentettek, félelmetes volt.
Bár szóban forgó pumpás része épnek látszott, Dobbertin nem akarta kockáztatni. Látása nem nagy, és aggódott amiatt, hogy szorosan figyelnie kell a készüléket, mert az bármikor megszakadhat - főleg, hogy a jótállása már lejárt. Korábban súlyos, alacsony vércukorszintű inzulinreakciói voltak, amikor arra ébredt, hogy a mentősök ott állnak fölötte, és ezt nem akarta újra megtapasztalni.
"Kifejeztem, hogy egyszerűen nem fogok élni attól a félelemtől, hogy véletlenül túladagolom magam hatalmas mennyiségű inzulinnal, ahogy valakivel (esetleg) már megtörtént egy ismert hiba miatt" - mondta.
A szivattyú cseréjének kezdeti vonakodása ellenére a felügyelő végül néhány napon belül küldött egy csereeszközt. Dobbertin elégedett az ügyének kezelése során nyújtott szolgáltatással, annak ellenére, hogy a 670G-t nem látszott befolyásolni ez a kérdés.
Nincs egyedül, mivel a Medtronicot már a visszahívási hírek kezdeteiben elárasztja a több száz hívás. Az online tapasztalataikat megosztó PWD-k vegyes érzelmeket fejeznek ki e felidézés komolysága kapcsán, egyesek megjegyzik, hogy ez "nem nagy ügy", mások pedig komoly aggodalmat fejeznek ki.
New York D-Mom: "Szerencsés, hogy kitért a golyó elől"

A New York-i Rochesterben található D-Mom Wanda Labrador szerint családját érintette ez a legújabb Medtronic visszahívás, de szerencsére abbahagyták a használatát, még mielőtt a társaság tavaly ősszel kiadta volna a sürgősségi biztonsági értesítést.
Labrador fiát Justice-t 3 éves korában diagnosztizálták a 2012. évi hálaadás napján, és azt a nyarat követõen elkezdte használni a Minimed kék színû inzulinpumpáját. Végül, miután sokáig várta a zárt hurkú technológia ígéretét, a Justice 2018 júliusában elindította a 670G szivattyút.
Néhány hónapon belül Wanda azt mondja, észrevette, hogy a rögzítőgyűrű gyakran meglazul, és rendszeresen meg kell húznia. Ez mindaddig folytatódott, míg végül elkopott és apró volt, és 2018 karácsony estéjén felhívta a Medtronicot, hogy jelezze a károkat. Másnap kaptak egy cserepumpa (boldog karácsonyt?). 5 hónappal később azonban azt mondja, hogy ugyanez történt megint; a rögzítőgyűrű levált és eltűnt.
Sokan mások az online eszközcsevegő csoportokban hasonló problémákról számoltak be, és azt mondták, hogy felhívták a céget erről - néha cserét kaptak, de gyakran hallották az ügyfélszolgálat meglepődését, majd azt mondták nekik, hogy ez nem aggasztó dolog.
"Úgy éreztem, hogy valami nincs rendben a szivattyúval, annak ellenére, hogy a Medtronic soha nem küldött figyelmeztetést a laza vagy hiányzó gyűrű veszélyére" - mondja. "Volt, amikor az egész víztározó csak kicsúszott ... ez nem volt rendben!"
Aggódva, de azért, hogy egy kis szünetet tartson magától a pumpaterápiától, Justice abbahagyta a 670G használatát, és a nyári hónapokban visszatért az injekciókhoz. Végül cukorbeteg táborba ment, és megismerte az Omnipodot és a Dexcomot, és annak ellenére, hogy továbbra is garanciális Medtronic szivattyúval rendelkezik, biztosításuk jóváhagyta az új eszközöket. Ennek ellenére a Labrador technikailag még mindig garanciális ügyfél a Medtronic-nál, de nem kapott levelet vagy értesítést erről a rögzítőgyűrű meghibásodásáról.
"Amikor megláttam a média tudósítását, szerencsésnek éreztem magam, hogy kitértem egy golyó elől, és hogy a fiamat soha nem bántották" - mondja. „Ugyanakkor felidegesítettem, hogy ennyi időbe telt, amíg a közvélemény megismerte az esetleges károkat, amelyeket a kérdés okozhat. Az emberek élete a tét, és nem igazságos, hogy a szivattyúkat korábban nem hívták vissza. Jobban kell teljesíteniük.
A termék visszahívása befolyásolja az egészségbiztosítási fedezetet?
Az olyan nagy biztosítók, mint az Anthem és a Blue Cross Blue Shield, azt mondják nekünk, hogy figyelembe veszik a visszahívási információkat. De a DiabetesMine egyik biztosítója sem beszélt a legutóbbi cukorbetegség-visszahívást követő héten, és nem jelezte, hogy tényleges adatok állnak rendelkezésre arról, hogy a biztonsági kérdések milyen gyakran merülnek fel, vagy hogy intézményük hogyan használhatja fel ezeket az információkat a fedezeti döntések meghozatalakor.
A Medtronic által a UnitedHealthcare (UHC) „előnyben részesített márkaszerződésével”, amely korlátozza a tagok hozzáférését a nem Medtronic diabéteszes eszközökhöz, egyesek elgondolkodtak azon, hogy az UHC észreveszi-e a preferált márka ezen I. osztályú visszahívását.
Az UHC kommunikációs igazgatója, Tracey Lempner szerint a Medtronic 2019-ben értesítette a biztosítót erről a kérdésről, amely kihat a Minimed 600 inzulinpumpa sorozatra.
Az UHC ezt követően nyilatkozatot adott ki az érintett tagok számára, amely így hangzott: „Tagjaink biztonsága kiemelt fontosságú, és mindenkit arra biztatunk, akinek kérdései vagy aggályai vannak az inzulinpumpa kapcsán, forduljon orvosához és forduljon a Medtronic-hoz további információkért. Továbbra is szorosan együttműködünk a Medtronic-nal, valamint figyelemmel kísérjük a legfrissebb klinikai bizonyítékokat annak biztosítására, hogy cukorbeteg tagjaink továbbra is hozzáférjenek a biztonságos, megfizethető ellátáshoz. "
Kíváncsiak lennénk bármilyen adatra, hogy az emberek milyen gyakran vetnek fel termék-visszahívási problémákat a lefedettségi kérelmeikben és a fellebbezéseikben, és hogy a biztosítók mit tesznek ezzel kapcsolatban.
Hogyan reagálnak az orvosok az orvosi termékek visszahívására?
Arra is kíváncsi voltunk, hogy az orvosok és a cukorbetegséggel foglalkozó szakemberek hogyan kezelhetik a betegek termékbiztonsági problémákkal kapcsolatos aggályait, és többekkel megkérdeztük, mit tanácsolhatnak valakinek, aki szembesül azokkal a gondokkal. A téma meglehetősen következetes: Esetenként, az adott terméktől vagy gyógyszertől és az érintett problémától függően. Gyakran az orvosok közvetlenül a céghez fordulnak további információkért és a szükséges segítségért.
"Igyekszünk proaktívak lenni, és megnézzük, vajon valóban veszélyt jelent-e a pácienseinkre" - mondta Dr. Jennifer Dyer, ohiói gyermek endokrinológus.
„Elég türelmesek vagyunk (ezek a problémák), mivel tudjuk, hogy gépek, és időnként megbízhatatlanok lehetnek, ezért mindig arra tanítjuk betegeinket, hogy okosabbak legyenek, mint a gépek. Gyakorlatunkban rendkívül alapos programunk van, amely ezen az elven alapul, ezért szerencsére a pácienseink általában rendben vannak, amikor ezek a dolgok történnek. Ebben a legutóbbi esetben a betegeinknek jól kell lenniük a protokolljainknak megfelelően - magyarázza.
Texasban az endokrinológus és a cukorbetegség szerzője, Dr. Stephen Ponder azt mondja, hogy az esetleges visszahívásokat is megbeszéli a betegekkel, és lehetővé teszi számukra, hogy hogyan tovább. Előfordul, hogy egy adott problémával kapcsolatban kapcsolatba akarnak lépni egy céggel, míg máskor a betegek abban bíznak, hogy nincs hibásan működő eszközük, és szívesen használják tovább.
"Tapasztalatom szerint a visszahívások egyszerűen az élet részei" - mondta. „Nem tudom, túl hamar rohanunk-e termékeket a piacra, vagy sem. A cukorbetegség terén jelenleg kifinomultabb felhasználói bázisunk van, mint a történelem bármikor, és ez a felhasználói bázis összekapcsolódik a közösségi médián keresztül. Ez lehetővé teszi a termékproblémák nagyobb és gyorsabb visszhangját, mint a 70-es, 80-as vagy 90-es években. "